肝癌是全球癌癥相關死亡的第三大原因,手術切除后的復發率高達70%,如何準確預測肝癌復發是一個難題。中國科學技術大學孫成研究組與合作者開發了預測肝癌復發的“TIMES”評分系統,通過量化免疫細胞在腫瘤微環境中的空間分布特征,實現了對肝細胞癌復發風險的預測,準確率達82.2%。他們將科學成果直接轉化為可應用的AI診斷工具——公開免費的TIMES在線版本,上傳病理染色圖像即可獲得肝癌復發風險評分。北京時間3月13日0點,該項成果發表在國際學術期刊《自然》上。
“TIMES”評分系統全稱為“Tumor Immune MicroEnvironment Spatial”(腫瘤免疫微環境空間)評分系統,是首個結合空間免疫信息的肝癌復發預測工具。研究證明了免疫細胞的空間分布比其整體數量更能決定臨床預后,將空間轉錄組學、蛋白質組學和多光譜免疫組化技術與人工智能驅動的空間分析整合,創造了腫瘤微環境評估的全新方法。
腫瘤微環境的空間異質性表現為不同腫瘤區域呈現差異化的免疫細胞組成。自然殺傷細胞(NK細胞)作為先天免疫系統的關鍵效應細胞,已有臨床數據提示腫瘤內NK細胞浸潤程度升高與患者生存預后顯著相關。然而,當前臨床評估體系主要依賴腫瘤特征的常規組織病理學分層方法,尚未整合免疫細胞在腫瘤微環境中的空間分布參數及其對預后的潛在影響。研究團隊發現CD57+NK細胞亞群在腫瘤微環境中的空間定位具有特殊的預后意義:腫瘤侵襲前緣區域CD57+NK細胞密度增高的患者表現出顯著降低的復發風險。
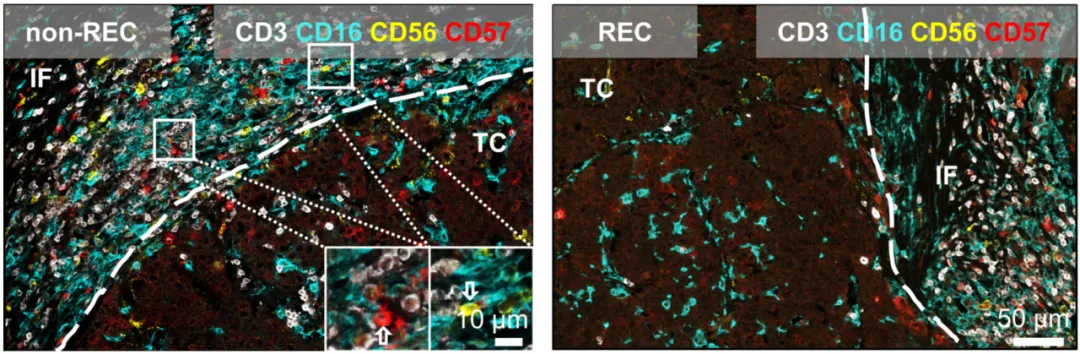
非復發(non-REC)和復發(REC)組織中的多色免疫組化染色。與復發肝癌相比,非復發肝癌患者的腫瘤侵襲前緣區域(invasive front)NK細胞更為豐富。
如何解釋NK細胞的分布與肝癌復發有關?研究團隊基于61名患者的肝癌切片進行了系統性的轉錄組-空間組學整合分析,解析多重免疫熒光高維數據,應用梯度增強機器學習算法模型鑒定了SPON2、ZFP36L2、ZFP36、VIM和HLA-DRB1這五個具有顯著預后意義的基因標記物,它們作為五個基本指標,構成了能有效預測肝癌復發的算法模型TIMES評分系統。
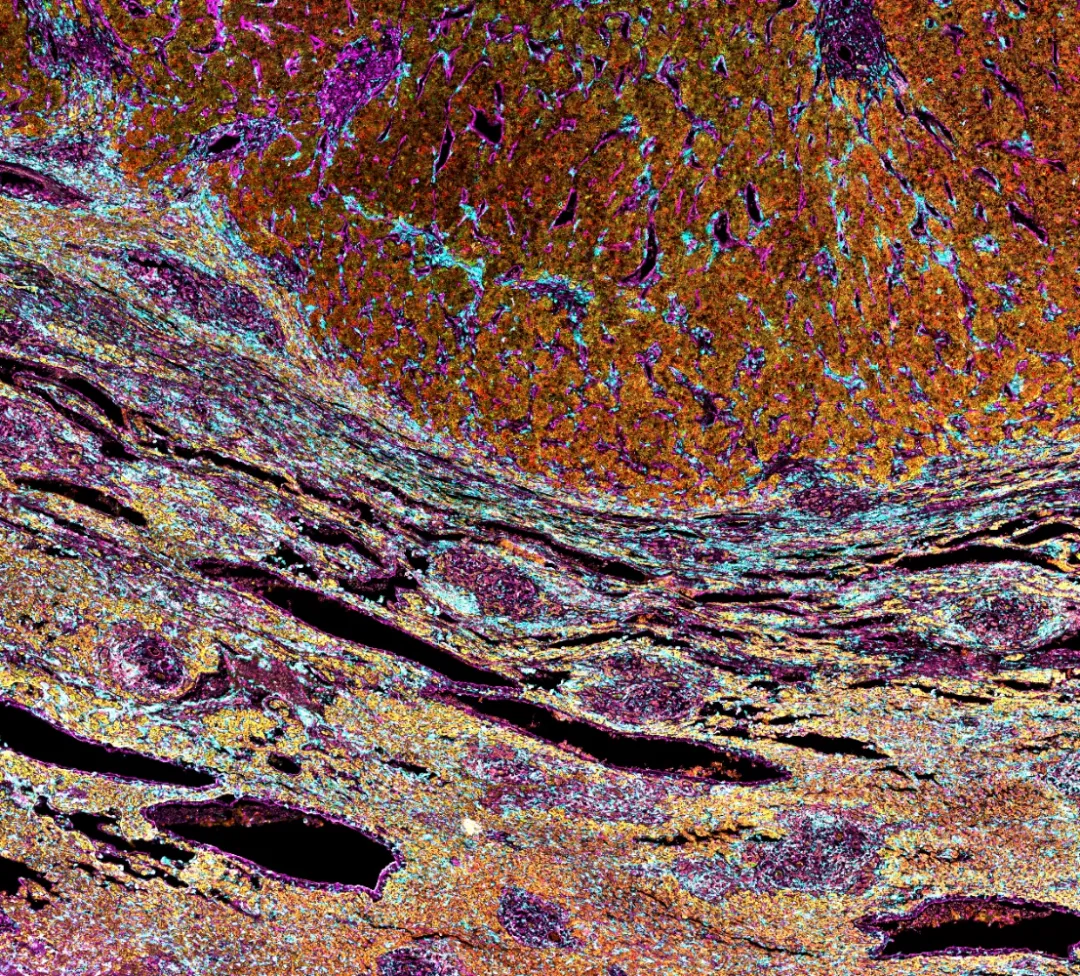
復發組織的代表性多色免疫組化圖像,顯示核染色(DAPI,藍色)和生物標志物:CD57(紅色),SPON2(綠色),HLA-DR(青色),ZFP36L2(黃色),ZFP36(橙色)和VIM(洋紅色)。
在231位患者的多中心驗證研究中,TIMES評分系統區分非復發和復發組織的準確率為82.2%,現有的肝癌臨床分期系統,如巴塞羅那分期、TNM分期系統的預測準確率在50%左右。
SPON2指標在TIMES評分系統中是最具預測性的。研究團隊針對SPON2指標的生物學意義開展了進步研究,通過3D打印實驗、殺傷實驗等,發現SPON2促進NK細胞的運動和向腫瘤細胞的定向運動,SPON2陽性NK細胞表現出更強的細胞毒性,并顯著增加細胞毒性T淋巴細胞的活化。隨后,研究者進一步建立NK細胞上SPON2特異性敲除小鼠的肝癌復發模型,發現SPON2增強免疫調節蛋白IFN-γ分泌和NK細胞浸潤,可以明顯抑制腫瘤的進展。這些說明SPON2陽性NK細胞能夠降低肝癌的復發風險。
為了方便臨床社區訪問TIMES系統,團隊開發了全球可用的在線網絡平臺(https://sun.times.ustc.edu.cn/),上傳患者肝癌組織的標準病理染色圖像或數據,即可獲得帶有TIMES評分和復發風險的報告。TIMES系統相關的核心算法和模型已獲得專利保護,研究團隊正積極尋求與企業合作,推動該預測系統的規范化臨床轉化應用。研究團隊希望能夠提供全新的臨床決策輔助工具,幫助醫生在有限資源條件下為患者制定最優化治療方案,讓預測肝癌復發的TIMES系統普惠可及。
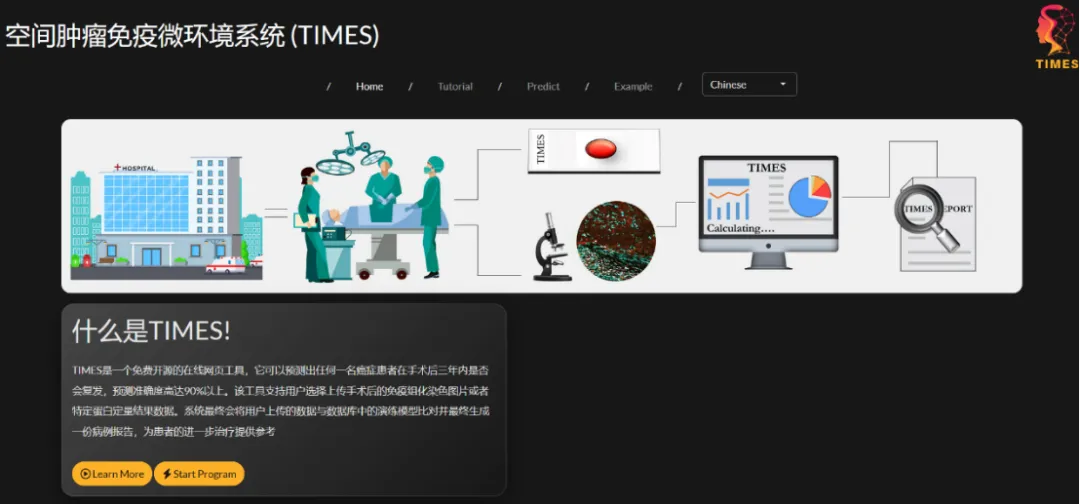
TIMES在線網絡平臺(https://sun.times.ustc.edu.cn/)
匹茲堡大學免疫治療領域知名專家Michael T. Lotze教授為該研究撰寫了深入的科學述評,強調這項研究“提供了令人信服的證據,證明空間免疫構架在肝細胞癌預后評估中具有首要地位”(provides compelling evidence for the primacy of spatial immune contexture in prognosticatings hepatocellular carcinoma),“建立了一個方法學框架,可廣泛應用于實體腫瘤,通過精確的空間免疫分析指導免疫治療干預”(establishes a methodological framework that could be broadly applicable across solid tumor malignancies, potentially guiding immunotherapeutic interventions through precise spatial immune profiling)。
中國科學技術大學孫成教授、中國科學技術大學劉連新教授、新加坡科學技術研究局Joe Yeong教授為本文的共同通訊作者;賈耿介教授(中國農科院基因組所)、賀培崎博士(中國科學技術大學)、戴天力博士生(中國科學技術大學)、Denise Goh研究員(新加坡科學技術研究局) 為本文的共同第一作者。該工作還得到了其他團隊成員的大力幫助。
論文鏈接:https://www.nature.com/articles/s41586-025-08668-x
① 凡本站注明“稿件來源:中國教育在線”的所有文字、圖片和音視頻稿件,版權均屬本網所有,任何媒體、網站或個人未經本網協議授權不得轉載、鏈接、轉貼或以其他方式復制發表。已經本站協議授權的媒體、網站,在下載使用時必須注明“稿件來源:中國教育在線”,違者本站將依法追究責任。
② 本站注明稿件來源為其他媒體的文/圖等稿件均為轉載稿,本站轉載出于非商業性的教育和科研之目的,并不意味著贊同其觀點或證實其內容的真實性。如轉載稿涉及版權等問題,請作者在兩周內速來電或來函聯系。





 中國教育在線
中國教育在線



